|
Körper: Nieren |
Die Niere (lat. ren, Adjektiv renal; griech. nephros) ist ein paarig angeordnetes Organ der Wirbeltiere. Eine Aufgabe der Nieren ist die Ausscheidung von überflüssigen Stoffen aus dem Körper, nämlich den Endprodukten des Stoffwechsels und die Ausscheidung von Giftstoffen durch Bildung des Harns.
Die Niere reguliert durch die Kontrolle der Zusammensetzung des Harns und über die Produktion von Hormonen den Wasserhaushalt, die Elektrolytzusammensetzung des Extrazellulärraums, den Blutdruck, den Säure-Basen-Haushalt, die Mineralisierung des Knochens, und durch Bildung des Hormons Erythropoetin auch die Blutbildung.
Die prinzipielle Funktionsweise der Niere besteht aus zwei Schritten: das Ultrafiltrat ohne Zellbestandtteile des Bluts wird gebildet und der grösste Teil dieser Flüssigkeit wird kontrolliert wieder in den Blutkreislauf zurück resorbiert.
Dabei wird zunächst aus dem Blut ein Ultrafiltrat abgepresst, das keine Zellen und nur noch sehr wenige grosse Proteine enthält. In diesem filtrierten Primärharn sind aber noch alle niedermolekularen Bestandteile enthalten, darunter solche, die ausgeschieden werden sollen, und auch solche, die für den Körper wertvoll sind, wie Glucose, Aminosäuren, Elektrolyte und insbesondere das Wasser. Im anschliessenden, schlauchartigen Tubulussystem werden daher diese Stoffe kontrolliert resorbiert und erst der entstandene Endharn über die ableitenden Harnwege ausgeschieden.
Makroskopische Anatomie
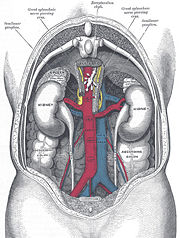
Lage
Beim Menschen liegen die Nieren retroperitoneal beiderseits der Wirbelsäule unterhalb des Zwerchfells, geschützt innerhalb einer Fettkapsel. Sie sind bohnenförmig und haben eine Länge von 10 bis 12 cm, eine Breite von 5 bis 6 cm und eine Dicke von 3 bis 5 cm (Merkwerte 4, 7, 4+7 oder auch 12 x 6 x 3). Das Gewicht variiert zwischen 120 und 200 g.
Beide Nieren sind jeweils von einer dünnen, festen, bindegewebigen Organkapsel (Capsula fibrosa) umhüllt und liegen zusammen mit den Nebennieren in einem Fettgewebskörper, der Capsula adiposa, eingebettet und abgepolstert. Die Capsula adiposa ist rückenseitig und seitlich stärker ausgebildet und von einem Fasziensack nach vorne, seitlich und hinten eingefasst, der nach medial oben und unten aber unverschlossen ist. Die Nieren haben - ausser unmittelbar zu den Nebennieren - getrennt durch die Fettkapsel Kontaktflächen zu mehreren Organen des Bauchraums. Die linke Niere wird von Magen, Milz, Pankreas und Colon descendens überlagert, die rechte vor allem von der Leber, aber auch von Colon ascendens und Duodenum. Wegen des Platzbedarfs der Leber ist die rechte Niere tiefer gelegen.
Jede Niere wird von meist einer (gelegentlich mehreren) direkt aus der Aorta entspringenden Arteria renalis mit Blut versorgt. Eine Vena renalis führt das Blut unmittelbar in die Vena cava inferior. Der Urin wird durch die beiden Harnleiter, die Ureteren, zur Harnblase transportiert.
Diese prinzipielle Lage ist auch bei den anderen Säugetieren typisch, hier liegen die Nieren (entsprechend der horizontalen Körperorientierung) hinter dem Zwerchfell. Bei den meisten Säugetieren liegt die rechte Niere etwas weiter vorn. Bei Wiederkäuern ist die linke Niere durch die Ausbildung des Pansens nach rechts, hinter die rechte Niere verlagert (physiologische Wanderniere).
Aufbau beim Menschen
Form des Organs und Lage der Gefässe
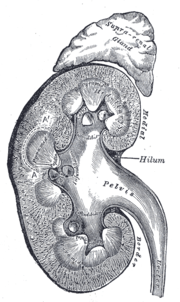
Beim Menschen zeigen die Nieren - ähnlich der Form einer Bohne - zwei Pole nach oben und unten, zwei Flächen nach vorne und hinten (ventral und dorsal) und zwei Ränder nach medial und lateral. Der nach aussen gerichtete Rand ist konvex, der nach medial gerichtete konkave Rand bildet eine Einziehung, in der das Hilum renale die Ein- und Austrittspforte der Leitungsbahnen darstellt. Hier verzweigen sich Vena und Arteria renalis und der Ureter, meistens in dieser Reihenfolge von ventral nach dorsal gelegen. Das Hilum erweitert sich in eine Ausbuchtung, den Sinus renalis, der von dem Nierenbecken und Fettgewebe ausgefüllt wird.
Innerer Aufbau
Das Nierenparenchym, die eigentliche Organmasse der Niere, wird in die aussen liegende Nierenrinde (Cortex renalis) und das nach innen zum Hilum gerichtete Nierenmark (Medulla renalis) unterteilt. Das Mark besitzt dabei die Form von Pyramiden (10 bis 12 Markpyramiden pro Niere), die mit ihrer Basis nach aussen und mit ihrer Spitze nach innen zum Hilum zeigen. Diese Spitzen, die Papillen, reichen frei in den Hohlraum der Nierenkelche (Calix renalis), die sich in variabler Form zum Nierenbecken (Pelvis renalis) zusammenschliessen, aus dem der Ureter hervorgeht. In dieser Anordnung fliesst der Urin aus den Papillen in Richtung Ureter.
Rinde und Mark
Die Nierenrinde liegt wie eine Kappe zwischen den Basen der Markpyramiden und der Organkapsel (subkapsulärer Anteil), erreicht aber zwischen den Pyramiden in säulenförmigen Abschnitten (Columnae renales) den Sinus renalis. Der subkapsuläre Anteil der Rinde wird von gut sichtbaren, feinen Strichen durchzogen, den Markstrahlen (Radii medullares), die radiär aus den Markpyramiden in Richtung der Organkapsel ausstrahlen und Teil des Marks sind. Im Mark selbst lassen sich durch ihre leicht unterschiedliche Farbe ein äusseres Mark, bestehend aus einem Aussen- und einem Innenstreifen, und ein zum Nierenbecken gelegenes inneres Mark unterscheiden.
Gefässverlauf
Die Arteria renalis teilt sich schon im Bereich des Hilus im Regelfall in zwei Äste auf (Ramus anterior und posterior), der Ramus anterior teilt sich wiederum in vier Segmentarterien. Der Ramus posterior versorgt ein Segment an der Hinterseite, so dass insgesamt fünf Nierensegmente entstehen.
Aufgrund der embryonalen Entwicklung, bei der die Niere im Bauchraum aufsteigt, sich alte Gefässe zurückbilden und neue die Versorgung übernehmen, sind Variationen relativ häufig. Von akzessorischen Nierenarterien spricht man bei einer zusätzliche Arterie, die in den Hilus mündet, von einer aberranten Arterie, wenn das Gefäss nicht am Hilus, sondern unabhängig oft an einem Pol mündet.
Nierentypen der Säugetiere
Bei den einzelnen Säugetieren ist die Niere unterschiedlich aufgebaut. In der einfachsten Form besteht die Niere aus einzelnen, kegelförmigen Nierenlappen (Lobi renales). Diese mehrlappige Niere ist typisch für Meeressäugetiere und Bären. Jeder Nierenlappen besteht aus einer Rindenkappe und einer Markpyramide, die in einer Nierenpapille (Papilla renalis, das spitze Ende des Kegels) endet.
Bei den meisten Säugetieren verschmelzen diese Nierenlappen (beim Menschen 6 Lappen) in unterschiedlichem Ausmass. Die verschmelzenden Rindenkappen bilden die Nierenrinde (Cortex renis), die Pyramiden das Nierenmark (Medulla renis).
Bei Rindern verschmelzen nur die Mittelteile der einzelnen Nierenlappen, wodurch an der Oberfläche Furchen entstehen und die Nierenpapillen ebenfalls erhalten bleiben. Diese Bauform nennt man mehrwarzig-gefurchte Niere. Diese Form tritt zwischenzeitlich auch in der fetalen Entwicklung der Niere bei den Säugetieren auf, die durch weitere Verschmelzungsvorgänge gekennzeichnet sind. Auch das menschliche Neugeborene besitzt noch eine mehrwarzig-gefurchte Niere.
Bei Primaten (einschl. Mensch) und Schweinen verschmelzen die Rindenanteile nach der Geburt vollständig, so dass die Organoberfläche glatt erscheint. Die einzelnen Papillen bleiben jedoch erhalten. Man spricht von einer mehrwarzig-glatten Niere.
Bei den meisten Säugetieren verschmelzen nun auch die einzelnen Nierenpapillen zu einer Nierenleiste (Crista renalis), so dass man von einer einwarzig-glatten Niere spricht.
Feinbau
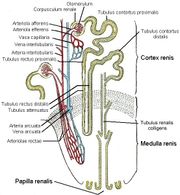
Der Feinbau der Niere zeichnet sich durch ein hochdifferenziertes Tubulussystem und eine spezifisch angepasste Blutversorgung aus. Das Tubulussystem lässt sich aufgrund der Embryonalentwicklung in zwei Teile gliedern, das Nephron im engeren Sinne, und das Sammelrohr. Beide bilden jedoch eine funktionelle Einheit, so dass der Begriff Nephron häufig auch das gesamte Tubulussystem bezeichnet.
Blutversorgung der Niere
Verzweigungen
Die Segmentarterien (siehe oben) teilen sich weiter auf. Eine Arteria interlobaris versorgt je zwei angrenzende Markpyramiden und entsprechende Rindenbereiche. Sie verläuft in den Rindensäulen entlang der Seiten der Pyramiden in Richtung Rinde, verzweigt sich aber an der Basis der Pyramide in Arteriae arcuatae. Diese verlaufen bogenförmig an der Mark-Rinden-Grenze und geben in rechtem Winkel die radiär nach oben durch die Rinde verlaufenden Arteriae corticales radiatae, auch Arteriae interlobulares, ab.
Erstes und zweites Kapillarbett
Aus diesen gehen schliesslich die Vasa afferentia hervor, die sich zu je einem Kapillarknäuel, dem Glomerulus (siehe unten), aufteilen. Aus diesem ersten Kapillargebiet läuft das immer noch sauerstoffreiche Blut wieder im Vas efferens zusammen. Von dort tritt das Blut in ein zweites Kapillarbett ein, diesmal zur Versorgung des Nierengewebes. Dabei muss man zwei Fälle je nach Lage des Glomerulus unterscheiden: aus oberflächlichen Glomeruli, die im oberen Bereich der Rinde zur Organkapsel hin liegen, gelangt das Blut in das peritubuläre Kapillarnetz der Rinde, das die dort gelegenen Tubuli umspinnt. Aus juxtamedullären Glomeruli jedoch, die tiefer zur Mark-Rinden-Grenze hin liegen, entspringen die Gefässe zur Versorgung des Marks.
Die Versorgung des Marks
Diese kapillären Gefässe zur Versorgung des Marks sind die Vasa recta, die ganz gerade oft bis zur Papillenspitze absteigen und wieder in umgekehrter Richtung aufsteigen. Es gibt zahlreiche Querverbindungen zwischen ab- und aufsteigendem Schenkel. Die besondere Gefässarchitektur des Marks ist von grosser funktioneller Bedeutung für die Fähigkeit der Niere zur Harnkonzentrierung. Im Rahmen des Gegenstromprinzips erzeugt die Niere zur Papillenspitze hin einen erheblichen osmotischen Gradienten (siehe unten), der ausgewaschen würde, wäre das Mark mit einem normalen Kapillarnetz versorgt. Der Preis dafür ist aber eine sehr schlechte Sauerstoffversorgung des Nierenmarks, da der Sauerstoff aus dem sauerstoffreichen, absteigenden Schenkel der Vasa recta direkt schon oben in den aufsteigenden, sauerstoffarmen Schenkel diffundieren kann.
Venöses System
Beide Kapillarnetze erreichen schliesslich das venöse System der Niere, das mit Ausnahme der Glomerula und ihren afferenten und efferenten Arteriolen, dem arteriellen System analog aufgebaut ist.
Nephron
Die Niere besteht aus zahlreichen Einheiten, den Nephronen, in denen der Harn gebildet wird. Jede der menschlichen Nieren enthält 1 bis 1,2 Mio. Nephrone. Das Nephron selbst besteht aus einem Nierenkörperchen (Corpusculum renis) und einem Tubulusapparat (Tubuli).
Im Nierenkörperchen befindet sich das Glomerulum, ein Gefässknäuel, durch dessen gefensterte Kapillarwände der Primärharn abfiltriert wird. Der Primärharn tritt aus dem Nierenkörperchen in den proximalen Tubulus und in die Henlesche Schleife über, wo er nach dem Gegenstromprinzip aufkonzentriert wird. Es folgen der distale Tubulus und ein Sammelrohr (Tubulus renalis colligens).
Neben der Ausscheidungsfunktion spielt die Niere auch eine Rolle in der Regulation des Blutdrucks und der Blutbildung. Im juxtaglomerulären Apparat wird abhängig von der Durchblutung das blutdrucksteigernde Enzym Renin gebildet (Goldblatt-Effekt). Auch die Sauerstoffkonzentration wird in der Niere registriert und über die Ausschüttung des Erythropoetins gesteuert, das die Produktion der roten Blutkörperchen stimuliert.
Funktion
Aufgaben der gesunden Niere
Die Niere ...
- reinigt das Blut von Abfallstoffen, die durch Stoffwechselvorgänge entstehen (z.B. Harnsäure, Harnstoff).
- reguliert den Säure-Basen-Haushalt des Körpers. Der pH-Wert des Blutes darf nur in sehr engen Grenzen schwanken, ansonsten wird es „sauer“ oder „alkalisch“; sowohl das eine als auch das andere führt letztlich zum Tod.
- reguliert den Gehalt an Körpersalzen (Natrium, Kalium, Calzium).
- reguliert den Blutdruck.
- ist durch die Bildung des Hormons Erythropoetin an der Blutneubildung beteiligt.
- erzeugt die so genannten renalen Hormone Cholecalciferol, Erythropoetin, Kinine und Prostaglandine.
- ist am Vitamin D-Stoffwechsel beteiligt.
- reguliert den Wasserhaushalt des Körpers.
Messung der Nierenleistung
Die Funktion der Niere kann anhand der Urinmenge, der Urinkonzentration und der Konzentration der harnpflichtigen Substanzen (Kreatinin, Harnstoff, Harnsäure, Kalium) im Blut abgeschätzt werden.
Die genaue Leistung der Nieren wird über die Clearance ermittelt. Hierzu gibt es verschiedene Verfahren:
- Die renale Clearance ist ein Mass für die Eliminierung eines Stoffes aus dem Blutplasma, man misst also die Klärfunktion der Niere. Sinkt die Clearance ab, d.h. nimmt die Leistung der Niere ab, spricht man von Niereninsuffizienz.
- Die Inulin-Clearance misst das Filtrationsvermögen der Niere. Hierzu wird dem Patienten Inulin verabreicht und gemessen, wie viel vom verabreichten Stoff pro Zeit wieder ausgeschieden wird. Da Inulin zwar filtriert, nicht aber rückresorbiert wird, ist die Inulin-Clearance identisch mit der glomerulären Filtrationsrate (GFR). Für den gesunden Jugendlichen liegt der Wert bei etwa 125 ml/min. Eine Abnahme des Wertes deutet auf eine Störung in der Nierenfunktion hin (Niereninsuffizienz). Mit zunehmenden Alter nimmt die GFR physiologisch auf 60-65 ml/min ab. Dies ist bei der Dosierung von Arzneistoffen, die über die Niere ausgeschieden werden, wichtig, da bei älteren Patienten durch die geringere GFR oft eine Verringerung der Dosis vorgenommen werden muss.
- Die Creatinin-Clearance wird wegen ihrer einfacheren Durchführung in der Klinik der Inulin-Clearance vorgezogen. Es wird die Ausscheidung von Creatinin gemessen, die annähernd der von Inulin entspricht. Die Creatinin-Plasmaspiegel, deren Wert von der Muskelmasse abhängt, schwanken nur wenig, was diese Messung überhaupt erst möglich macht. Vorteilhaft ist weiterhin, dass die Infusion, die bei der Messung der Inulin-Clearance erforderlich ist, entfällt.
Autoregulation der Nierendurchblutung
Die treibende Kraft des Filtriervorgangs ist der in den Glomerulumgefässen herrschende Blutdruck. Der Blutdruck des Körpers unterliegt normalerweise im Verlauf des Tages typischen Schwankungen: Im Schlaf ist er niedriger als z. B. bei körperlicher Anstrengung oder bei Stress. Auch bei bestimmten Erkrankungen, z. B. Diabetes mellitus oder Hypertonie, ist der Blutdruck erhöht. Für die Filtration in den Glomeruli ist aber ein konstanter Blutdruck wichtig. Deshalb hat die Niere die Fähigkeit, den Blutdruck in ihrem Innern ihren Bedürfnissen anzupassen. Man nennt das auch Autoregulation der Niere.
Die Autoregulation erfolgt mit Hilfe von Druckrezeptoren, die in den zu- und abführenden Blutgefässen des Nierenkörperchens sitzen. Bei zu hohem Blutdruck werden die zuführenden Arterien weiter gestellt und sorgen so für einen konstanten Blutdruck in den dahinterliegenden Gefässen des Nierenkörperchens. Ist der Blutdruck zu niedrig, so werden die von Glomerulus abgehenden Gefässe enger gestellt. Das erhöht den Blutdruck im Glomerulum auf den gewünschten Wert.
Normale Blutdruckschwankungen bleiben ohne Auswirkung auf die Nieren. Auf diese Weise können Schwankungen des systolischen Blutdrucks zwischen 80-180 mmHg ohne grosse Auswirkungen auf die Filtrationsvorgänge der Nieren bleiben. Darüber hinaus können die Nieren aufgrund ihrer empfindlichen Drucksensoren den Blutdruck ständig überwachen und bei Schwankungen regulierend eingreifen (vgl. Blutdruckregulation der Nieren).
Tubuloglomerulärer Feedback (TGF)
Als Tubuloglomerulärer Feedback (TGF) bezeichnet man einen Mechanismus, mit dem die Filtration eines einzelnen Nephrons in der Niere reguliert wird.
Bei Zunahme des NaCl-Gehalts im distalen Tubulus (Mittelstück) kommt es über eine Sensorfunktion der Macula densa, einem Teil des juxtaglomerulären Apparats, zu einer Reduktion der glomerulären Filtrationsrate desselben Nephrons. Dies wird durch eine vom Mesangium vermittelte Vasokonstriktion (Gefässverengung) der zum Nierenkörperchen hinführenden Arteriolen (Vasa afferentia) realisiert und dadurch eine Verminderung der glomerulären Filtrationsrate erzielt.
Genaugenommen handelt es sich hierbei um einen physiologischen Regulationsmechanismus, der das Einzelnephron vor Hyperfiltration schützen soll und bei einem akutem Nierenversagen „fälschlicherweise“ dadurch aktiviert wird, dass die NaCl-Resorption durch die tubuläre Schädigung stark beeinträchtigt wird. Dies führt zu einer erhöhten Flussrate im distalen Tubulus und/oder zu einem erhöhten NaCl-Angebot im Bereich der Macula densa, was schliesslich zur Auslösung des tubuloglomerulären Feedbacks führt.
Untersuchungsmethoden der Niere
- Laboruntersuchungen
- Urinuntersuchung
- Teststäbchen auf Bakterien, Eiweiss, Blut, Zucker etc.
- Urinsediment
- Blutuntersuchung
- Kreatinin
- Kalium
- Harnstoff
- Harnsäure
- Steinuntersuchungen
- Urinuntersuchung
- Bildgebung
- Ultraschall
- Röntgen Kontrastmitteldarstellung der Niere = iv-Pyelogramm
- CT der Niere
- Magnetresonanztomografie der Niere
- Angiografie der Niere
- Nuklearmedizinische Verfahren
- Statische Nierenszintigrafie
- Nierenausscheidungsszintigrafie
- Nierenperfusionsszintigrafie
Krankheiten der Niere
Krankhafte Veränderungen des Nierengewebes können die Glomerula (Glomerulonephritiden) oder die Nierentubuli (Tubulointerstitielle Nierenerkrankungen) betreffen. Bei ersteren spielen mehr autoimmune Prozesse eine Rolle, bei letzteren Intoxikationen und Infektionen (akut v.a. bakterielle Infektionen). Daneben können beide durch autoimmune oder metabolische Systemerkrankungen mitbetroffen sein. Genetisch bedingte Erkrankungen betreffen meist die Funktion der Tubuli. Die verschiedenen Prozesse unterscheiden sich klinisch kaum, man unterscheidet zwischen akutem und chronischem Nierenversagen bzw. akuten und chronischen Glomerulonephritiden. Sie führen unbehandelt zu Glomerulosklerose und Niereninsuffizienz mit Dialysepflichtigkeit. Es gibt auch Anlagefehler, Nierentumore, Nierensteine.
Eine schwere Schädigung der Nieren hat andererseits Störungen der Blutdruck- und Hormonregulation des Organismus zur Folge. Es kommt zu Renaler Hypertonie, renalem Vitamin D - Mangel und sekundärem Hyperparathyreodismus, bei schwerer chronischer Niereninsuffizienz zum Urämischen Syndrom mit Organschäden und u.a. Juckreiz. Die Schädigungen können evtl. durch salz- und eiweissarme Ernährung und viel Trinken verlangsamt werden oder die Dialysetherapie wird notwendig.
Nierenkrankheiten: Systematik
- Glomerulonephritiden / Glomerulopathie (Autoimmunentzündung der Nieren)
- akut (mit Nephritischem Syndrom)
- Rapid Progressive Glomerulonephritis
- Postinfektiöse Glomerulonephritis
- chronisch (mit Nephrotischem Syndrom)
- IgA-Nephritis
- Minimal-Change-Glomerulonephritis
- Fokal-Segmentale Glomerulonephritis, siehe unter Nephrotisches Syndrom
- membranoproliferative Glomerulonephritis, evtl. durch ein Alport-Syndrom (Defekt des Typ IV-Kollagens, geht einher mit Hämaturie, progredientes Nierenversagen und Innenohrschwerhörigkeit)
- membranöse Glomerulonephritis
- akut (mit Nephritischem Syndrom)
- Tubulointerstitielle Nierenerkrankungen
- akut
- bakteriell Pyelonephritis (Nierenbeckenentzündung)
- viral (Hantaan-Virus)
- parainfektiös (Streptokokken‚ EBV)
- allergisch/toxisch
- chronisch
- Analgetikanephropathie und andere Intoxikationen/Überempfindlichkeitsreaktionen
- Sarkoidose
- akut
- Systemerkrankungen mit Nierenbeteiligung
- Vaskulitiden (autoimmune Gefässentzündungen)
- Morbus Wegener
- Lupus erythematodes
- Purpura Schönlein-Hennoch
- Andere Gefässveränderungen
- Hypertensive Nephropathie
- HUS/TTP
- Metabolische Beeinträchtigungen
- Diabetische Nephropathie
- Amyloidose
- Multiples Myelom
- Gicht
- Vaskulitiden (autoimmune Gefässentzündungen)
- Erbliche Nierenkrankheiten
- tubuläre Funktionsstörungen
- Bartter-Syndrom (selten)
- Fanconi-Syndrom
- Renal-tubuläre Azidose
- Phosphatdiabetes
- angeborener renaler Diabetes insipidus
- Diabetes renalis
- Zystinurie
- Balkan-Nephritis
- Gitelman-Syndrom
- Morbus Fabry
- Anatomische Anlagefehler
- Doppelniere
- Zystennieren oder Familiäre Zystennieren, medizinisch: Polyzystische Zystennieren (PKD)
- Hufeisenniere
- Markschwammniere
- tubuläre Funktionsstörungen
- Nierensteine und Nephrokalzinose
- Nierenabsenkung (umgangssprachlich „Wanderniere“)
- Krebs
- bösartig: Nierenzellkarzinom
- gutartig: z.B. Angiomyolipom
Dieser Artikel stammt aus der freien Enzyklopädie Wikipedia und kann dort eingesehen werden (Autorenliste). Der Artikel steht unter der GNU Lizenz für freie Dokumentation.
Unsere Website dient einzig Informationszwecken. Sie ersetzt keinesfalls die persönliche Untersuchung, Beratung und Behandlung durch Fachkräfte. Bitte beachten Sie auch unsere Rechtlichen Nutzungsbedingungen.
[an error occurred while processing this directive]
