|
Krankheiten: Lyme-Borreliose |
|
| Klassifikation nach ICD-10 | |
|---|---|
| A69.2 | Lyme-Krankheit Erythema chronicum migrans durch Borrelia burgdorferi |
| ICD-10 online (WHO-Version 2006) |
Die Lyme-Borreliose oder Lyme-Krankheit ist eine Infektionskrankheit, die durch das Bakterium Borrelia burgdorferi aus der Gruppe der Spirochäten ausgelöst wird. Der Erreger Borrelia burgdorferi ist eng verwandt mit Treponema pallidum, dem Erreger der Syphilis. Die Borrelien ziehen sich schon bald nach der Infektion aus dem Blutkreislauf in das Gewebe zurück. Es kann jedes Organ, das Nervensystem, die Gelenke und das Gewebe befallen werden. Deshalb spricht man bei dieser Erkrankung auch von einer multisystemischen Krankheit. Die Erkrankung kommt beim Menschen und allen anderen Säugetieren sowie Vögeln vor. Die Übertragung erfolgt vor allem durch den Holzbock, eine Zeckenart, sehr selten auch durch Stechmücken oder Pferdebremsen.[1]
Entdeckung und Namensgebung
Die Bezeichnung „Lyme-Borreliose“ setzt sich zusammen aus dem Namen des Ortes Lyme im US-Bundesstaat Connecticut, in dem das Krankheitsbild 1975 nach gehäuftem Auftreten von Gelenksentzündungen in Verbindung mit Zeckenstichen erstmals beschrieben wurde, sowie aus der Bezeichnung der Erkrankung als Borreliose, die auf die mikrobiologisch-systematische Einteilung des Erregers zurückgeht. Der Erreger wurde als Borrelia burgdorferi nach seinem Entdecker Willy Burgdorfer, einem Schweizer, benannt, der die Bakterien 1981 in den USA entdeckte.
Erreger

Von dem krankheitsverursachenden Bakterium Borrelia burgdorferi kommt in den USA im Wesentlichen nur eine einzige Borrelien-Spezies vor. In Europa existieren hingegen sechs verschiedene humanpathogene Genospezies. Bestimmte Erkrankungsformen, wie beispielsweise die ACA, kommen zwar in Europa, aber nicht in den USA vor. Dies sind in Europa B. burgdorferi sensu stricto, B. garinii, B. afzelii, B. valaisiana, B. lusitaniae und B. spielmani (A14S). Bis auf B. lusitaniae wurden alle Genospezies auch in Zecken in Deutschland gefunden. Die einzelnen Genospezies gelten auch als unterschiedlich komplement-resistent.
Statistik
Verbreitung
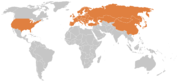
Der Erreger der Lyme-Borreliose ist weltweit verbreitet. In Deutschland gibt es ein Süd-Nordgefälle bei der Durchseuchung des Holzbocks. Während in den nördlichen Bundesländern die Zecken nur etwa zwischen 6 % bis 10 % mit Borrelia burgdorferi durchseucht sind, liegt die Durchseuchungsrate im süd- und mitteldeutschen Raum bei etwa 20 % bis 30 %. Regional liegt die Quote der infizierten Zecken bei bis zu 50 %. Allerdings fehlen aktuelle und ausreichend flächendeckende Studien in Deutschland.
Es fehlen flächendeckende epidemiologische Studien und Daten über die Ausbreitung und das Infektionsrisiko nicht nur der einzelnen Genospezies für den Menschen. Ebenso sind die Pathomechanismen, der Verlauf der einzelnen Krankheitsmanifestationen und deren Behandelbarkeit noch unzureichend erforscht. Im Gegensatz zur artverwandten Syphilis, der durch Läuse übertragenen Borrelia recurrentis sowie der ebenfalls durch Zecken übertragenen FSME wurde die Borreliose nicht in das Infektionsschutzgesetz aufgenommen. In den Neuen Bundesländern und Berlin besteht jedoch eine auf landesrechtlicher Ebene geregelte Meldepflicht für die Erkrankung Lyme-Borreliose. Hier werden die Falldefinitionen des Robert-Koch-Instituts zugrunde gelegt, die jedoch lediglich eine Meldung des Erythema chronicum migrans und der frühen Neuroborreliose vorsehen. Das Erythema migrans tritt jedoch nur in etwa 50 % der Neuerkrankungen auf. Wie entsprechende Daten aus anderen Ländern zeigen, wird die Meldepflicht auch nicht von jedem Arzt konsequent eingehalten. Es wird davon ausgegangen, dass deshalb nur etwa ein Viertel der tatsächlichen Fälle gemeldet werden. Mischinfektionen sind möglich, wobei mehrere Erregergattungen übertragen werden können. Da ausreichende Studien fehlen, ist die Datenlage über Mehrfachinfektionen unzureichend.
Infektionsrisiko und Durchseuchungsraten
Lyme-Borreliose ist in der nördlichen Hemisphäre die häufigste von Zecken übertragene Erkrankung. Eine Borrelieninfektion durch Zecken ist – im Gegensatz zu der durch Viren verbreiteten FSME – in ganz Deutschland und sogar in Städten möglich. Wie eine Studie am Max-von-Pettenkofer-Institut für Hygiene und Mikrobiologie in München zeigte, stellt „der direkte Kontakt mit Büschen in Gärten ein bisher unterschätztes Risiko“ dar, über Zeckenstiche an Lyme-Borreliose zu erkranken. Gleichwohl hat nicht jeder Zeckenstich eine Borrelieninfektion oder gar eine Erkrankung an Borreliose zu Folge. Nach Schätzung des Robert-Koch-Instituts liegt die Wahrscheinlichkeit, nach einer in Deutschland erlittenen Zeckenattacke an Borreliose zu erkranken, bei 1 zu 300. In Hochrisikogebieten dagegen muss man gemäss einer Studie der Universität Heidelberg von einer wesentlich grösseren Gefahr ausgehen: Bei etwa einem von zehn Betroffenen ist mit einer Erkrankung zu rechnen. Allerdings basieren diese Angaben lediglich auf Schätzungen, da zuverlässige Daten über das Erkrankungsrisiko nach einer erfolgten Infektion mit Borrelia burgdorferi fehlen. Die Übertragungsgefahr korreliert mit der Durchseuchungsrate der Zecken in den verschiedenen Regionen.
Die Durchseuchungsraten der Zecken mit Borrelien variieren je nach Region und reichen von ca. 5 bis weit über 40 Prozent. Im Mittel liegt die Befallsrate in Deutschland bei etwa 20 Prozent. Forscher gehen in Hochrisikogebieten, wie z. B. in Teilen von Süddeutschland, von 30 bis 50 Prozent borreliendurchseuchter Zecken aus. In der Region Konstanz am Bodensee lag die mittlere Infektionsrate der Zecken mit Borrelien (B. burgdorferi Spezies) bei 35 Prozent. Im Englischen Garten und den Isarauen in München waren etwa 30 % der gefundenen Zecken mit Borrelien verseucht.
Aufgrund der seit Anfang 2001 bestehenden Meldepflicht in Berlin und den Neuen Bundesländern wurden aus diesem Gebiet zwischen 2002 und Ende 2006 23.394 Erkrankungen an das Robert-Koch-Institut gemeldet. [2] Dies entsprach im Jahr 2002 einer Häufigkeit von 17,8 Fällen pro 100.000 Einwohner; mit zunehmender Meldefreudigkeit der Ärzte stieg die Inzidenz (Zahl der in einer Bevölkerung neu auftretender Erkrankungen pro Jahr) auf 37,3 Erkrankungsfälle pro 100.000 Einwohner im Jahr 2006. Rund 70 Prozent aller gemeldeten Fälle traten in den Monaten Juni bis September auf.
Über die Zahl der Neuinfektionen bzw. Neuerkrankungen pro Jahr gibt es für Gesamt-Deutschland wegen der in den Alten Bundesländern fehlenden Meldepflicht nur Schätzungen, die je nach Studie stark variieren und von 50.000 bis 160.000 Fällen ausgehen. Die Inzidenz für Borreliose variiert dementsprechend von 0,06 Prozent bis 0,2 Prozent (zum Vergleich: die Inzidenz für FSME ist etwa 500 mal geringer). Das Landesgesundheitsamt Stuttgart geht nach einer an der Universität Heidelberg an 3708 Patienten durchgeführten Studie davon aus, dass in den Borrelien-Hochendemiegebieten etwa jeder zehnte Zeckenstich zu einer Infektion führt. Hierbei wurde eine Transmissionsrate von 25 Prozent bei infizierten Zecken (3,5 % total) zu Grunde gelegt.
Die Universität Heidelberg hat in einer Studie das Infektionsrisiko nach einem Zeckenstich ermittelt: Hiernach infizieren sich im Durchschnitt drei Prozent aller von durchseuchten und nicht durchseuchten Zecken gestochenen Personen. Wird man jedoch von einer mit B. burgdorferi durchseuchten Zecke gestochen, so liegt die Gefahr sich zu infizieren gemäss dieser Studie bei 27 Prozent. Andere Studien gehen von über 35 Prozent aus.
In einem 1998 von führenden Borrelioseforschern in Deutschland publizierten Konsensuspapier findet man folgende Angaben zur Erkrankungswahrscheinlichkeit nach einem Zeckenstich (Angaben für Gesamtdeutschland, unabhängig davon ob die Zecken infiziert waren oder nicht):
- eine Serokonversion, also das Ansprechen des Immunsystems auf den Erreger nach Infektion, ist bei 2,6–5,6 % der Betroffenen zu erwarten
- eine manifeste Erkrankung jedoch nur bei 0,3–1,4 %.
Zuverlässige Zahlen hierzu gibt es nicht. Legt man aber diese Zahlen zugrunde, kann man davon ausgehen, dass 25 bis 50 % Prozent der mit Borrelien infizierten Personen im weiteren Verlauf auch an Borreliose erkranken. Zurzeit wird noch erforscht, ob die unterschiedlichen Genospezies von Borrelia burgdorferi ursächlich für die verschiedenen Krankheitsbilder sind. Diese werden von den Ärzten möglicherweise nicht immer korrekt als "Borreliose" diagnostiziert.
Eine prophylaktische einmalige Gabe von Antibiotika - zumindest nach einer Zeckenattacke in einem Hoch-Risiko-Gebiet - wird von einigen Forschern empfohlen. Diese Empfehlung stammt aus den USA, wo es nur eine Genospezies gibt und ist deshalb in Europa sehr umstritten. Um das Infektionsrisiko nach einem Zeckenstich besser abschätzen zu können, kann die Zecke gegebenenfalls auf Borrelienbefall mittels PCR-Untersuchung untersucht werden. Eine Durchseuchung mit Borrelien ist jedoch nicht mit einer Krankheitsübertragung gleichzusetzen. Denn die Zecke benötigt für die Übertragung der Borrelien – anders als bei dem FSME-Virus – einige Zeit. Die Angaben darüber schwanken zwischen 6 und 48 Stunden. Fest steht jedoch: Je länger eine borreliendurchseuchte Zecke gesaugt hat umso höher ist das Risiko einer Übertragung. Ein Teil der Infektionen erfolgt aber auch durch das unsachgemässe Entfernen der Zecke, wenn diese gequetscht wird.
Zecken sollten so schnell wie möglich entfernt werden. Hierzu bieten sich spezielle Pinzetten an, die vorzugsweise aus Edelstahl gefertigt sein sollten (siehe auch ausführlich unter Zeckenstich).
Übertragung

Überträger des Bakteriums sind in der Regel Zecken, die den Erreger beim Saugen nach einigen Stunden (in der Regel in einem Zeitfenster von 8 bis 12 Stunden nach dem Einstich) auf den Menschen übertragen. In Deutschland ist das vor allem die Zecke Ixodes ricinus, auch Gemeiner Holzbock genannt. Zecken sind weltweit Überträger von mehr als 50 Krankheiten (siehe Zeckenstich).
Als weitere Überträger der Borreliose werden von Wissenschaftlern auch Stechmücken diskutiert, wobei in bisherigen Studien[3][4] nur eine sehr geringe Durchseuchung von Mücken festgestellt wurde. Parasitologen der Universität Bonn sind in letzter Zeit der Frage nachgegangen, ob Laufmilben (Trombiculidae), darunter die in Deutschland heimische Herbstmilbe (Neotrombicula autumnalis), als Vektoren für das Bakterium Borrelia burgdorferi infrage kommen, es ergaben sich aber keine konkreten Hinweise. Allerdings ist hier unklar, ob diese Spinnentiere tatsächlich in der Lage sind, Borrelien auf den Menschen zu übertragen. Bekannt ist jedoch eine Übertragung durch Bremsen[5].
Eine direkte Übertragung der Borrelien von Mensch zu Mensch ist nicht bekannt, d. h. erkrankte Personen sind nicht ansteckend. Dagegen besteht bei einer infizierten Frau in der Schwangerschaft die Gefahr von Totgeburten oder der Schädigung des ungeborenen Kindes. Eine Übertragung durch Blutprodukte ist zwar grundsätzlich möglich, wird aber bislang als unwahrscheinlich angesehen. Nach Auskunft des Robert-Koch-Instituts ist die Borreliose nicht sexuell übertragbar. Genügend aussagekräftige Studien fehlen hierzu jedoch.
Diagnose
Ein grosses Problem bei der Feststellung der Borreliose ist die laborchemische (serologische) Unterscheidung zwischen einer abgeheilten Borreliose (Seronarbe) von einer noch aktiven therapiebedürftigen Borreliose. Es kommt deshalb nach wie vor zu falsch negativen und falsch positiven serologischen Befunden. In der Serologie werden in der Routinediagnostik Antikörpertests eingesetzt. Das sind i.d.R. der ELISA und der Westernblot, auch Immunoblot genannt. Manche Labors führen auch einen Immunfluoreszenztest (IFT) durch. Solche Tests können nur die Antikörper messen, d.h. feststellen, ob ein Erregerkontakt stattgefunden hat oder nicht. Es ist jedoch durch diese Verfahren nicht möglich, den Krankheitsverlauf einer Borreliose zu kontrollieren. Deshalb ist auch nicht möglich, aufgrund der serologischen Ergebnisse nach einer Behandlung mit Antibiotika festzustellen, ob diese wirksam waren und die Borreliose nun ausgeheilt ist. Hinzu kommt, dass die einzelnen Testverfahren nicht standardisiert sind und eine unterschiedliche Spezifität und Sensitivität aufweisen. Bei sehr sensitiven Tests besteht oftmals das Problem von sogenannten Kreuzreaktionen. Das bedeutet, der Test zeigt ein positives Borrelien-Ergebnis an, der Betreffende hat aber keine Borreliose (Alpha-Fehler, falsch-positiv). Das wird durch andere Erreger, wie zum Beispiel durch andere Spirochäten wie Treponema pallidum oder Treponema denticola, Leptospiren, aber auch durch das Epstein-Barr-Virus oder Zytomegalievirus verursacht. Genauso kommen falsche negative Ergebnisse vor (Beta-Fehler). Die Serologie ist vor allem in den frühen Phasen nicht zuverlässiger als 50 %. Neuere Tests sollen inzwischen eine etwas höhere Zuverlässigkeit aufweisen, die mit einer Sensitivität von ca. 70 bis 80 % angegeben wird. Allerdings sind dies Angaben der jeweiligen Labors, die nicht überprüft wurden.
Es werden gerade in der Frühphase viele Borreliose-Fälle übersehen, da innerhalb der ersten Wochen noch keine messbaren Antikörperspiegel gegen Borrelienantigene gebildet werden (sogenannte diagnostische Lücke = Zeitpunkt von der Infektion bis zur ersten Antikörperproduktion). Daher sollte in Frühstadien nicht das Ergebnis einer Blutuntersuchung abgewartet werden, sondern unverzüglich bei entsprechendem klinischen Verdacht antibiotisch therapiert werden, da bei frühzeitiger Behandlung die Heilungschancen am grössten sind. Eine sogenannte Wanderröte (Erythema migrans) muss sofort behandelt werden. Auch bei einer floriden Borreliose können Entzündungsparameter wie BKS, CRP und andere akute-Phase-Proteine unauffällig bleiben, so dass normale Werte dieser akute-Phase-Proteine (Entzündungsparameter) nicht geeignet sind, eine aktive Borreliose auszuschliessen.
In späteren Stadien ist die Sensibilität der serologischen Testmethoden (ELISA) in der Regel höher. Sie soll im zweiten Stadium bei etwa 70 % bis 90 % liegen. Bei einem Verdacht auf eine manchmal klinisch wenig spezifische Neuroborreliose ist in der Regel eine Liquoruntersuchung angezeigt, bei der durch Feststellung entzündlicher Liquorveränderungen und den Nachweis einer borrelienspezifischen intrathekalen Antikörpersynthese sich gegebenenfalls ein solcher bestätigen lässt.[1] Allerdings kann es hierbei bei ca. 30 % zu falschen negativen Ergebnissen kommen. Im Frühstadium der Neuroborreliose ist oftmals noch keine Infektion mit Borrelien nachweisbar. In diesen Fällen könnte das kürzliche entdeckte Chemokin CXCL13 (ein B-Lymphozyten anziehendes Protein) eine wichtige Rolle spielen, da es bereits in Frühstadien der Erkrankung im Liquor von Patienten mit Neuroborreliose deutlich erhöht ist. Nach der bisherigen Studienlage ist die Spezifität dieses Markers mit der intrathekalen Antikörpersynthese vergleichbar. Darüber hinaus sinkt die Konzentration von CXCL13 im Liquor unter Behandlung rasch ab und hilft somit eine aktive Infektion von einer Seronarbe zu unterscheiden. Bislang ist dieser Marker jedoch noch nicht in der klinischen Diagnostik etabliert, sondern wird nur im Rahmen von Studien (z. B. an der Universitätsklinik der LMU München) untersucht. Auch wenn lediglich eine Beteiligung peripher Nerven vorliegt, kann die Liquordiagnostik negativ sein. Die Zuverlässigkeit der Liquordiagnostik ist auch von der Erfahrung des Labors, zugrunde gelegten Kriterien für die Auswertung, Präparationszuverlässigkeit sowie den verwendeten diagnostischen Verfahren abhängig. In Deutschland sind zahlreiche Borrelien-Serologien mit unterschiedlichen Antigenkompositionen auf dem Markt, die eine grosse Bandbreite hinsichtlich der Sensitivität und Spezifität aufweisen. Deshalb kann es vorkommen, dass mit einem Test negativ und mit einem anderen positive Ergebnisse festgestellt werden. Es besteht weder eine Genehmigungspflicht für die Borrelien-Serologie, noch ist eine Teilnahme an Ringversuchen verpflichtend.
In einigen spezialisierten Labors und Instituten wird bei positiver Serologie und fraglicher Erregeraktivität der LTT (Lymphozytentransformationstest) durchgeführt. Dieser Test gehört seit 2005 zu den in Deutschland akkreditierten Laborverfahren zum Nachweis zellulärer T-Zellreaktivitäten. Ein positives Ergebnis deutet auf Borrelien-spezifische T-Zellen im Blut hin und unterstützt den klinischen Verdacht auf eine aktive Borreliose. Dass wirklich eine enge Korrelation zwischen einem positiven LTT und der Krankheitsaktivität besteht, ist allerdings bislang in grösseren klinische Studien nicht untersucht. Der LTT wird seit April 2006 von den Gesetzlichen Krankenkassen nicht mehr übernommen. Der PCR-Nachweis stellt eine weitere Diagnosemethode dar, mit der eine aktive Borreliose festgestellt werden kann. Hier wird aus dem Erreger DNA aufgearbeitet und mittels der PCR-Reaktion ein borrelienspezifisches Fragment vervielfältigt (amplifiziert). Dieser Test ist hochspezifisch, stellt gleichzeitig aber hohe Anforderungen an Laborpersonal und -ausrüstung. Die Sensitivität ist stark abhängig vom untersuchten Körpermaterial (Liquor bei einer Neuroborreliose etwa 20–30 %, Synovialflüssigkeit bei einer Lyme-Arthritis und Haut bei einer Dermato-Borreliose etwa 70 %). Ein negatives Ergebnis schliesst eine aktive Borreliose deshalb nicht aus. Wenn Kontaminationen sowie tote Erreger ausgeschlossen werden konnten, ist ein positives Ergebnis ein Hinweis auf eine aktive Borreliose. Der Direktnachweis von Borrelien(-DNA) aus Zecken mittels PCR wird von verschiedenen Firmen bzw. Laboren angeboten. Die Kosten für die von den Krankenkassen nicht getragene Leistung liegen je nach Anbieter zwischen 10 und 100 Euro. Ein positiver Nachweis in der Zecke besagt nicht, dass auch im Menschen eine Infektion stattgefunden hat! Als alleiniger Nachweis für eine Borrelieninfektion wird dieser Test von keiner Fachgesellschaft empfohlen. Andere Aussagen sind nicht korrekt und sollten kritisch hinterfragt werden. Somit sind Therapien, die sich alleinig auf diesen Befund ohne Symptome und Serologie berufen, nicht indiziert.
In der Regel wird eine sogenannte Zwei-Stufen-Testung durchgeführt. Es wird erst ein ELISA eingesetzt, der jedoch Kreuzreaktionen bzw. polyklonale Antikörperstimmulierungen durch andere Krankheitserreger aufweisen und deshalb falsch-positiv sein kann. Das Ergebnis wird durch einen Immuno- bzw. Westernblot verifiziert und bestätigt. Bei negativem ELISA-Test und fortbestehendem klinischen Verdacht auf eine Borreliose empfiehlt sich die Durchführung eines Westernblot.
Differentialdiagnose
In Abhängigkeit vom Krankheitsstadium ist die Differenzialdiagnose weit gefächert. Es empfiehlt sich, weitere durch Zecken übertragene Erkrankungen und andere Infektionen (Babesiose, Rickettsiose, Leptospirose, Bartonellose und andere) auszuschliessen.
Die Borreliose kann, ähnlich wie eine Lues, eine Vielzahl von Erkrankungen „imitieren“. Es ist bei einer neurologischen Beteiligung an andere Ursachen, insbesondere Infektion mit neurotropen (auf die Nerven wirkende) Viren und Bakterien zu denken. Wichtig ist bei neurologischen Beschwerden die zuverlässige Abgrenzung gegenüber einer multiplen Sklerose, um eine schwerwiegende Fehlbehandlung mit Steroiden anstatt mit Antibiotika zu vermeiden. Bei Gelenkentzündungen kommen die aktivierte Arthrose, die rheumatoide Arthritis und andere Gelenkentzündungen in Frage. Eine Abgrenzung der Lyme-Enzephalopathie von einem Chronischen Erschöpfungssyndrom ist häufig schwierig.
Weitere wichtige Differenzialdiagnosen – insbesondere bei erfolgloser Therapie – sind Tumoren und andere Systemerkrankungen.
Krankheitsverlauf
Nach einer Infektion kann es zur Bildung von Antikörpern gegen Borrelien kommen, ohne dass es gleichzeitig zu Krankheitssymptomen kommt. Die Serologie kann noch Jahre nach einer ausgeheilten Borreliose positiv sein. Eine sichere Diagnose kann oft anhand der Krankheitssymptome, des Krankheitsverlaufs, der Krankengeschichte und der serologischen Befunde gestellt werden. Bei Unklarheiten kann manchmal ein Behandlungsversuch mit Antibiotika Klarheit bringen. Allerdings besagt das Ansprechen auf die Antibiotikagaben nicht, dass eine aktive Borreliose vorliegt, und umgekehrt belegt ein Nicht-Ansprechen nicht, dass die Krankheit ausgeheilt ist. Welches die optimale Therapie gegen Borreliose darstellt, ist umstritten.
In der Regel äussert sich eine Lyme-Borreliose durch schwere Symptome, die sich im Laufe der Jahre verschlimmern. Symptomfreie Latenz-Zeiten sind allerdings möglich. Ein Verschwinden der Symptome bedeutet deshalb nicht, dass die Erreger eliminiert sind. In der Frühphase sind die Symptome einer Borreliose einem grippalen Infekt (ohne Husten und Schnupfen) ähnlich. In diesem Stadium kommt es häufig zu Myalgien und Arthralgien, die mit einer Fibromyalgie verwechselt werden können. Dieselben Symptome werden auch oft nach einer Antibiotikabehandlung beschrieben. Wenn Symptome wie bei einer Fibromyalgie oder einem Chronic-Fatigue jedoch gleich bleiben und ohne Antibiotikagaben keine Verschlechterung eintritt, muss man eher davon ausgehen, dass die Beschwerden nicht durch Borrelia burgdorferi verursacht werden, vor allem, wenn in der Vorgeschichte keine borreliosetypischen Leitsymptome aufgetreten sind. Dies gilt auch für andere unspezifische Symptome wie Schüttelfrost, Fieber, Gelenk- und Muskelschmerzen, Erschöpfungszustände und Depressionen.
Nach einer durchgemachten Borreliose besteht keine Immunität.
Stadien
Es gibt eine Reihe von Symptomen, die für die einzelnen Stadien typisch sind. Daneben kann sich die Borreliose aber zusätzlich durch eine Vielzahl von unspezifischen Beschwerden wie Müdigkeit, Kopfschmerzen, Fieber, Nackensteifigkeit, Sehbeschwerden, Schwindel, Übelkeit und Erbrechen sowie psychische Veränderungen manifestieren.
1. Stadium: Lokalinfektion
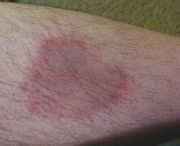
Ab Übertragung des Erregers kann es nach einer Inkubationszeit von meist 5 – 29 Tagen zu einer Lokalinfektion der Haut kommen, die mit einem charakteristischen Hautausschlag, dem Erythema migrans (Wanderröte) einhergeht.[6] Das Erythem verschwindet manchmal ohne Therapie, kann aber auch über Monate bestehen. Ein Rückgang des Erythema migrans ist kein Beleg für eine Heilung, da der Erreger gestreut haben kann. Es dehnt sich meist langsam um die Einstichstelle einer Zecke aus (daher der Name). Das Erythema migrans (Wanderröte) ist ein eindeutiges Symptom für eine Borrelieninfektion. Es fehlt allerdings bei mehr als der Hälfte der Erkrankungen. Im ersten Stadium kann die Borreliose noch gut mit Antibiotika (Doxicyclin) behandelt werden. Notwendig ist jedoch eine ausreichend lange und hoch genug dosierte Therapie. Was ausreichend ist, ist in der Wissenschaft umstritten.
2. Stadium: Streuung des Erregers
Nach etwa 4 bis 16 Wochen [7] breiten sich die Erreger im ganzen Körper aus. Die Inkubations- und Latenzzeit kann auch länger sein. Der Patient leidet dann an grippeähnlichen Symptomen wie Fieber und Kopfschmerzen, was die Erkennung der Krankheit erschwert. Charakteristisch sind starke Schweissausbrüche. Durch die Ausbreitung im Körper kann es zu einem Befall der Organe, der Gelenke und Muskeln sowie des zentralen und peripheren Nervensystems kommen. Leitsymptome in diesem Stadium sind oftmals das Bannwarth-Syndrom mit starken radikulitischen Schmerzen und eine Facialisparese, die sich in einem schiefen Gesicht zeigt. Typisch sind auch von Gelenk zu Gelenk springende Arthritiden und Myalgien. Weiterhin kann es zu Störungen des Tastsinns, Sehstörungen und Herzproblemen, wie Sinustachykardien und Karditis kommen, was sich manchmal durch Herzklopfen und hohen Blutdruck sowie Pulsbeschleunigung bemerkbar macht. Das Immunsystem ist in diesem Stadium oft nicht mehr in der Lage, die Infektion zu bewältigen. Borrelien scheinen sich nur kurz im Blut aufzuhalten und sich sehr schnell im Bindegewebe festzusetzen. Hier sind sie vom Immunsystem und durch Antibiotika nur schwer zu eliminieren.
Ein problematischer Sonderfall ist die sogenannte Neuroborreliose, die zu vielfältigen Erkrankungen der peripheren Nerven und bei circa 10 % der Erkrankungen auch des Zentralnervensystems führen kann. In aller Regel tritt sie in der frühen Erkrankungsphase auf (bis etwa 10 Wochen), in der noch keine Antikörper gebildet wurden. Deshalb müssen in diesem Stadium ausreichend Antibiotika gegeben werden. Die Wahl des Antibiotikums richtet sich nach dem Befall und der Erkrankungsform. Wenn die Borreliose nicht rechtzeitig und ausreichend behandelt wird, so kann die Erkrankung fortschreiten und zu bleibenden Organschäden führen.
3. Stadium: chronische Infektion
Wenn die Borreliose nicht rechtzeitig behandelt wird, kann es zu einer Erregerpersistenz und damit zu einer chronischen Infektion kommen (Spätmanifestation). Das heisst, die Krankheit kommt immer wieder (rezidiviert) oder verschlechtert sich zunehmend. Monate-, aber auch jahrelange symptomfreie Latenzzeiten mit anschliessenden Wiederaufflackern der Erkrankung sind möglich. So tritt die Akrodermatitis chronica atrophicans Herxheimer (ACA) oft erst nach Jahren auf. Es kann auch zu einer chronischen rezidivierenden Lyme-Arthritis mit vielfältigen Krankheitsbildern kommen oder auch zu einem Befall des zentralen und peripheren Nervensystems (Neuroborreliose) mit Polyneuropathie, Borrelien-Meningitis, Lyme-Enzephalomyelitis oder einer Enzephalitis. Ebenso sind chronische Erkrankungen der Sinnesorgane und der Gelenke und Muskeln möglich. Die chronischen Erkrankungen der Gelenke werden Lyme-Arthritis genannt. Es kann aber auch zu einer entzündlichen Bursitis oder Arthrose kommen. Die unterschiedlichen Erreger scheinen verschiedene Krankheitsbilder auszulösen: Während bei einem Teil der Patienten fast nur die Gelenke betroffen sind, kommt es bei anderen hauptsächlich zu neurologischen Störungen. Daneben gibt es auch eine Gruppe von Patienten, die Herzprobleme meist verbunden mit Gefässentzündungen haben. Mischformen sind möglich. Viele Borreliose-Patienten klagen über unerträgliche Erschöpfung, rasche Erschöpfbarkeit und chronische Müdigkeit, die sich auch durch ausreichend Schlaf nicht beseitigen lässt.
In der Fachliteratur werden vor allem späte Manifestationen der Lyme-Borreliose beschrieben:[8]
Chronisch rezidivierende Lyme-Arthritis
- Arthritis mit Befall der grossen Gelenke
- Tenosynovitis, Fasziitis, Osteomyelitis, Pannikulitis, Daktylitis, Bursitis usw.
- Arthralgien, Myalgien (Fibromyalgie-ähnliche Symptome?)
Neurologische, neuropsychiatrische Erkrankungen
- Radikulitis spinaler Nerven und Hirnnerven
- Neuritis peripherer Nerven
- Meningitis
- Myelitis
- zerebrale Vaskulitis
- Myositis, dermatomyositisartige Verläufe
- Enzephalitis, Enzephalopathie (chronic-Fatigue-ähnliche Symptome?)
Acrodermatitis chronica atrophicans (ACA)
- Stadium infiltrativum mit ödematösen Schwellungen (Erythromelalgie)
- atrophes Stadium mit zigarettenpapierartiger Verdünnung der Haut
- sklerodermieartige Verhärtung der Haut und fibröse Knoten
Weitere mögliche Spätfolgen
- Post-Treatment-Lyme-Syndrom (Post-Lyme-Syndrom ?)
- Erkrankung des Herzens: u. a. Myokarditis und Kardiomyopathie
- Erkrankung des Hörsystems, u. a. Tinnitus und Schwerhörigkeit
- Erkrankung der Augen: u. a. Uveitis, Keratitis, Episkleritis
- Erkrankung der Leber, der Nieren sowie des Magen- und Darmtrakts
Therapie
Die Behandlung einer Borreliose stellt auf Grund der Möglichkeit des vielfachen Organbefalls eine interdisziplinäre Herausforderung der verschiedenen Fachdisziplinen in der Medizin dar.
Die Verabreichungsform und Länge der Antibiotikatherapie richtet sich nach dem Krankheitsstadium, aber insbesondere nach der Krankheitsmanifestation. Hierbei sind individuelle Risikofaktoren der Patienten (wie z. B. eine Antibiotikaallergie oder eine Niereninsuffizienz u. a.) zu berücksichtigen. Je länger eine Borrelieninfektion dauert, umso schwieriger wird es, eine komplette Erregereliminierung zu erreichen. Für die Therapie stehen grundsätzlich verschiedene Antibiotika zur Verfügung. Es wird zwischen extrazellulären (ausserhalb der Körperzellen) und intrazellulären Erregern (in Zellen des Bindegewebes, des Knorpels, Fettgewebe und der Haut) unterschieden.
Dementsprechend sind die Antibiotika auszuwählen. Diese müssen auch "zellgängig" sein. Besonders Spätformen der Borreliose (persistierend) weisen intrazelluläre Erreger auf. Unterstützt wird die Zellengängigkeit durch gleichzeitige Gabe von Hydroxychloroquin, das einen basischen Zustand in den Zellen herbeiführt und das Eindringen des Antibiotikums in die Zellen unterstützt. Zellgängige Antibiotika sind Clarithromycin und Azithromycin in Kombination mit Hydroxychloroquin.
Ein extrazellulär wirkendes Antibiotikum ist Ceftriaxon, das intravenös über 14-21 Tage in einer Dosis von 2 g i. v. pro Tag gegeben wird. In einer Metaanalyse von acht europäischen Studien mit insgesamt 300 Patienten mit definitiver Neuroborreliose zeigte sich kein statistisch signifikanter Unterschied beim Behandlungserfolg zwischen einer oralen Doxycyclin-Therapie im Vergleich zur intravenösen Therapie mit Penicillin G oder Ceftriaxon (Neurology 69,2007,91). Es gibt keinen wissenschaftlichen Beleg, eine Behandlungsdauer von mehr als 14 bis 30 Tagen bei Patienten mit Lyme-Borreliose zu empfehlen.
Bei der Lyme-Enzephalopathie, einer schweren Hirnerkrankung, konnte eine aktuelle Studie allenfalls Kurzzeiteffekte durch Antibiotika nachweisen.[9]
Wie in den Empfehlungen der Deutschen Gesellschaft für Neurologie zur Neuroborreliose ausgeführt ist, ist die optimale Behandlungsdauer vor allem mit den intravenös zu verabreichenden Antibiotika Ceftriaxon und Cefotaxim unklar. Eine Behandlungsdauer über 3 Wochen ergibt jedoch keinen zusätzlichen Effekt. Inzwischen werden auch in fortgeschrittenen Stadien andere Antibiotika als Cephalosporine eingesetzt, u. a. Tetracycline, da die β-Lactam-Antibiotika (wie Ceftriaxon, Cefotaxim) im Verdacht stehen, sogenannte zystische oder zellwandlose Formen zu verursachen und bei intrazellulärer Persistenz nicht ausreichend zu wirken. Einige Behandlungsformen bestehen aus einer Kombination von intravenösen und oralen Antibiotika.
Während der Therapie, insbesondere wenn sie länger vorgenommen wird, ist eine enge Begleitung durch einen borreliosekundigen Arzt erforderlich. Insbesondere sollte eine engmaschige sonographische Kontrolle der Gallenblasenfunktion (bei der Anwendung von Ceftriaxon), der Leber- und Nierenwerte und des Blutbildes erfolgen. Bei Doxycyclin sind Milchprodukte, Calcium und Magnesium nur zeitversetzt einzunehmen. In seltenen Fällen wurde bei Doxycyclin eine Photosensibilisierung beobachtet; ein Sonnenexposition ist bei empfindlichen Hauttypen zu vermeiden. Fraglich ist, ob die Lyme-Borreliose im III. Stadium noch heilbar ist. Für eine Behandlung der Lyme-Borreliose mit Cholestyramin ergibt sich weder eine wissenschaftliche Rationale noch ergeben sich hierzu Argumente aus kontrollierten Studien. Eine solche Behandlung wird nicht empfohlen.
Patienten können ihre Erfahrungen in Selbsthilfegruppen austauschen. In der Regel können von den Gruppen auch borreliosekundige Ärzte genannt werden.
Vorbeugung
Zeckenstichvermeidung
Siehe Hauptartikel Zeckenstich
- Nach dem Besuch in Wald und Flur den Körper sorgfältig absuchen. Gefundene Zecken sorgfältig entfernen und diese dem Arzt zur Untersuchung mitbringen.
- Hohe krautige Vegetation meiden. Eine Übertragung kann auch im eigenen Garten und in kurzgeschnittenem Gras (Badewiese) erfolgen.
- Die Verwendung von entsprechenden Zeckenschutzmitteln (Repellentien) ist geeignet, das Risiko von Zeckenstichen zu verringern, und bietet einen relativen, jedoch keinen absoluten Schutz gegen Zeckenstiche. Die Wirksamkeit dieser auf die Haut aufgetragenen Zeckenschutzmittel liegt zwischen 4-6 Stunden. Bei der Anwendung entsprechender Repellentien sind die Herstellerhinweise zu beachten.
Immunisierung
Aktive und passive Immunisierungen stehen bisher für Europa nicht zur Verfügung. In den USA war für wenige Jahre ein wirksamer rekombinanter Impfstoff auf der Basis von OspA (äusseres Membranprotein von Bbsl) zugelassen, der aus kommerziellen Gründen vom Hersteller vom Markt genommen wurde. Wegen der Heterogenität der Stämme (mindestens 7 OspA-Serotypen) ist die Entwicklung eines wirksamen Impfstoffes für Europa schwierig, so das Robert-Koch-Institut 2007. In der Veterinärmedizin wird jedoch bei Hunden eine Impfung gegen Borrelien auch in Deutschland durchgeführt. Ihre Wirkung ist umstritten, da die durch die Impfung induzierten Antikörperspiegel rasch wieder abfallen und infolge des Vorhandenseins einer Vielzahl endemischer Borrelien-Stämme das Aufbauen kreuzreagierender und schützender Impftiter fraglich ist.
Grundsätzlich ist es möglich, die Bauanleitung der Eiweisse vieler Impfstoffe in pflanzliches Erbmaterial einzuschleusen, so dass derart veränderte Pflanzen zu Impfstoffproduzenten werden. Die von den Forschern derart veränderten Tabakpflanzen produzierten ein Ospa genanntes Eiweiss, welches sich ebenfalls auf der Oberfläche der Borreliose-Erreger findet. Eine zur Wirksamkeit zusätzlich notwendige Verknüpfung des genannten Eiweisses mit Fettsäuren wurde durch die Pflanzen ebenfalls erreicht. In Versuchen mit Mäusen erwies sich der so produzierte Tabak-Impfstoff im Vergleich zu aus Bakterienkulturen gewonnenem Impfstoff als ähnlich wirksam, jedoch ist dieser bislang noch nicht für den Menschen zugelassen [10]. Da jedoch in Europa ein für Menschen geeigneter Borreliose-Impfstoff in nächster Zukunft nicht zur Verfügung stehen wird, sind vor allem dringend weitere Forschungen zur Epidemiologie, zum Krankheitsverlauf, der Pathogenese, den diagnostischen Grundlagen und den therapeutischen Interventionen notwendig.
Einzelnachweise
- ↑ a b Leitlinie Neuroborreliose der Deutschen Gesellschaft für Neurologie bei AMWF online (Stand 2005)
- ↑ Robert Koch Institut: Epidemiologisches Bulletin Nr. 38 vom 21. September 2007, S. 351–355 Die für Tschechien ausgewiesene Inzidenz lautet für 2005: 36 Fälle pro 100.000 Einwohner
- ↑ Ann Agric Environ Med. 9, 2002, S. 55-57
- ↑ Folia Biologica. 54, 2006, S. 55-59
- ↑ The New England Journal of Medicine. 322, 1990, S. 1752
- ↑ AKH-Consilium - Lyme-Borreliose
- ↑ AKH-Consilium - Lyme-Borreliose
- ↑ Jutta Zacharias, Meissen, in www.zecken-borreliose.de
- ↑ Brian A. Fallon et al.: A randomized, placebo-controlled trial of repeated IV antibiotic therapy for Lyme encephalopathy. Neurology 2007 doi:10.1212/01.WNL.0000284604.61160.2d
- ↑ Nature Biotechnology Bd.24 S.76
Dieser Artikel stammt aus der freien Enzyklopädie Wikipedia und kann dort eingesehen werden (Autorenliste). Der Artikel steht unter der GNU Lizenz für freie Dokumentation.
Unsere Website dient einzig Informationszwecken. Sie ersetzt keinesfalls die persönliche Untersuchung, Beratung und Behandlung durch Fachkräfte. Bitte beachten Sie auch unsere Rechtlichen Nutzungsbedingungen.
[an error occurred while processing this directive]

